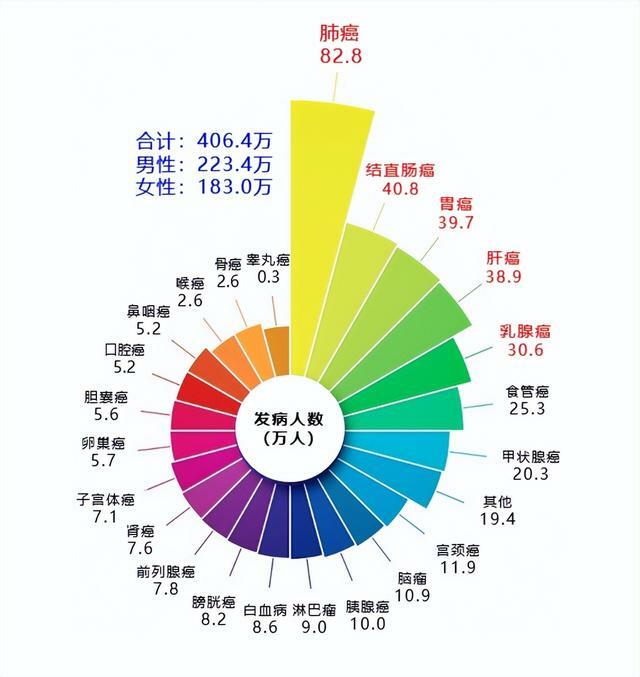
國家癌症中心於2022年發布了最新一期的全國癌症統計數據。根據《2022年全國癌症報告》,2016年,中國新發癌症病例數達406.4萬,相當於每天超1萬人被診斷出癌症,每分鐘有8個人患癌。癌症是危害人類健康的重大疾病,也是全球醫學界面臨的共同難題。2023年2月4日,是第24個世界抗癌日。作為我國最早興辦、享譽海內外的著名高等學府,西安交通大學面向世界科技前沿、面向人民生命健康,在多種癌症的防治方面產出了一系列高水平研究成果。
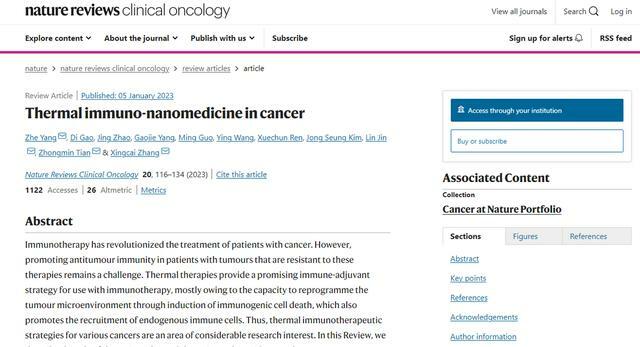
- 發表《熱療-免疫聯合治療納米藥物在癌症治療中的應用》
熱療是一種已在臨床廣泛應用的癌症治療手段,主要通過提高全身或腫瘤組織的溫度,利用熱作用及其繼發效應來治療惡性腫瘤。2023年1月5日,西安交通大學生命學院生物醫學光子學與傳感研究所楊哲、田中民教授團隊受邀在國際權威期刊《自然綜述·臨床腫瘤學》(Nature Reviews Clinical Oncology,IF:65.011)發表題為《熱療-免疫聯合治療納米藥物在癌症治療中的應用》(Thermal immuno-nanomedicine in cancer)綜述論文,系統闡述了抗腫瘤熱療-免疫聯合治療的臨床研究進展以及納米藥物助力該聯合治療的研究現狀與應用前景。論文第一作者為西安交大生命學院楊哲副教授,高迪副教授及西北大學化工學院趙婧副教授,第一單位為西安交大生命學院生物醫學信息工程教育部重點實驗室。
- 在頭頸部鱗狀細胞癌防治研究領域取得新進展
頭頸部鱗狀細胞癌(Head and Neck Squamous Cell Carcinoma,HNSCC)占惡性腫瘤的5%以上,儘管HNSCC的診治目前已有相當大的進展,但疾病總體生存率並沒有得以改善,究其原因與HNSCC復發和遠處轉移的特性有關,但具體的生物學過程和機制尚不清楚。目前越來越多的研究者認為異常的脂質代謝是包括HNSCC在內的許多癌症的標誌性特徵,肥胖和血脂升高都是HNSCC的危險因素。然而,HNSCC中涉及的脂質代謝依賴性分子機制仍然知之甚少。
在現有研究基礎上,西安交通大學口腔醫院李錦峰團隊通過闡釋HNSCC細胞生長轉移的機制,為HNSCC提供新的治療靶點,從而提升HNSCC的防治水平。研究成果以《SQLE表達上調可以促進頭頸鱗癌的惡性進展》(Upregulation of SQLE Contributes to Poor Survival in Head and Neck Squamous Cell Carcinoma)為題,發表於《國際生物科學雜誌》(International Journal of Biological Sciences)。

- 在功能材料的腫瘤高效靶向遞送研究領域取得重要進展
功能材料的高效靶向遞送是腫瘤等疾病實現精準治療的關鍵。大量相關研究表明,納米遞送系統能夠有效提升功能材料的血液長循環時間從而提升診療效果,但遞送過程中材料的過早泄露和非特異性靶向極大限制了遞送效率,亟待開發新型策略加以克服。針對以上關鍵問題,西安交通大學醫學部基礎醫學院吳昊研究員團隊、第二附屬醫院馬小斌副教授團隊和加州大學戴維斯分校李源培教授團隊提出一種利用硼酸酯鍵的「需求性」響應釋放納米遞送策略,進一步依據策略構建新型遞送系統(PO-PB@SPIOs),成功限制了材料遞送過程中的過早泄露並實現功能材料「需求性」的靶向投遞,顯著延長材料的血液長循環時間,極大提升材料在卵巢癌組織的富集效率,從而在實現對在體卵巢癌小鼠模型的高特異性近紅外螢光(nearinfrared fluorescence, NIRF)、核磁(magneticresonance, MR)成像診斷,並在診斷基礎上實施精準光熱治療達到80%的卵巢癌治癒率,其中避免材料過早泄露的特點使遞送系統整體展現出優異的生物安全性。
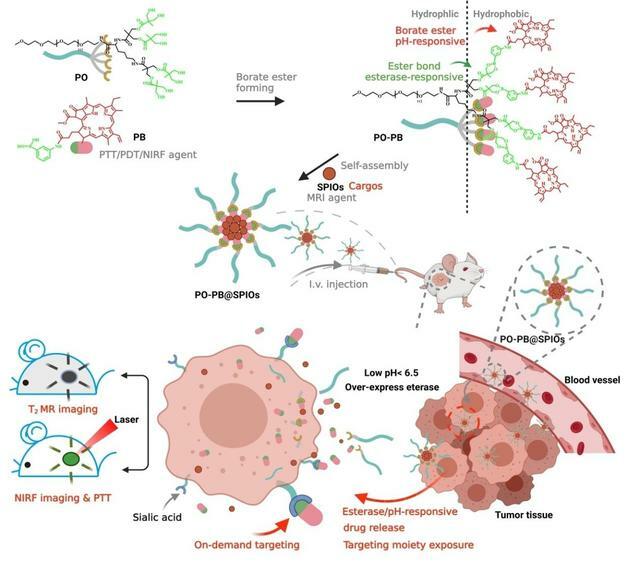
這項工作表明,利用硼酸酯鍵的「需求性」響應釋放納米遞送策略能夠在有效提升遞送效率的同時兼顧安全性,為未來設計構建面向臨床應用的診療材料遞送系統設計提供了一種具有參考價值的新策略。該項工作以《具有刺激響應釋放性能的「需求性」靶向納米診療策略用於提升癌症組織的材料遞送效應》(On-demand targeting nanotheranostics with stimuli-responsive releasing property to improve delivery efficiency to cancer)為題,發表於國際期刊《生物材料》(Biomaterials)。論文第一作者為課題組科研助理盧宏偉、碩士研究生徐徛(共一)和陝科大楊金帆副教授(共一),西安交通大學吳昊研究員、馬小斌副教授以及加州大學戴維斯分校李源培教授為共同通訊作者,西安交通大學為第一產權單位。本項工作具有開發新型藥物納米配方的巨大潛力,相關產品已經申報了國家發明專利。

- 提出指導中國癌症病人免疫療法用藥決策的突變負荷閾值精確優化方法
免疫檢查點抑制劑是近年來新興的一類抗腫瘤療法,大量中晚期、轉移性癌症患者從中受益。判斷一名患者是否適用免疫療法的核心指標是腫瘤突變負荷(TMB)。在臨床實踐中,針對不同的癌症,一般有不同的TMB閾值;若患者的TMB高於閾值則建議用藥。然而,如何立足中國癌症病人的特點,準確、全面地獲得適用於中國人群的TMB閾值是臨床實踐中的一個突出問題。

針對上述問題,西安交通大學計算機科學與技術學院生物信息管理與數字健康研究團隊與中山大學腫瘤防治中心、南京世和基因生物技術股份有限公司合作,設計了一套面向多癌種、多分組、多終點的TMB閾值精確優化方法及其對應的通用統計學框架。在此基礎上,針對現有的生物信息學工具在分析隊列數據時產生的嚴重樣本間偏差,研究人員基於機器學習理論解釋了偏差構成因素,並首次通過基因區間的分類集成框架有效控制了樣本間偏差,能夠顯著提高臨床決策的準確度。近期,上述研究成果分別發表在國際免疫學領域權威期刊《免疫學前沿》(Frontiers in Immunology)、知名期刊《遺傳學前沿》(Frontiers in Genetics),並獲得第十七屆中國管理學年會優秀論文獎。
- 開發出子宮內膜細胞人工智慧輔助診斷系統
子宮內膜癌是女性生殖道三大惡性腫瘤之一。子宮內膜癌細胞學篩查存在病理醫師缺乏、診斷難等痛點及難點。基於長期子宮內膜細胞學研究積累,西安交大一附院婦產科李奇靈教授團隊在2018年開始和西安交大自動化學院鍾德星副教授團隊合作,將人工智慧應用於子宮內膜細胞學診斷。利用深度學習方法對26,880個子宮內膜細胞patch進行訓練,並在11,520個patch的測試集中進行測試。訓練集可達到100%的準確率,測試集獲得了93.5%的準確率、92.2%的特異性和92.0%的敏感性。並開發了子宮內膜細胞醫學圖像分析軟體,結合李教授前期發明成果轉化的子宮內膜取樣、製片系統,形成了準確、快速、自動識別的子宮內膜細胞人工智慧輔助診斷系統。該系統可大幅降低醫生的工作強度,提升病理醫生工作效率,適用於大規模開展篩查和診斷工作。
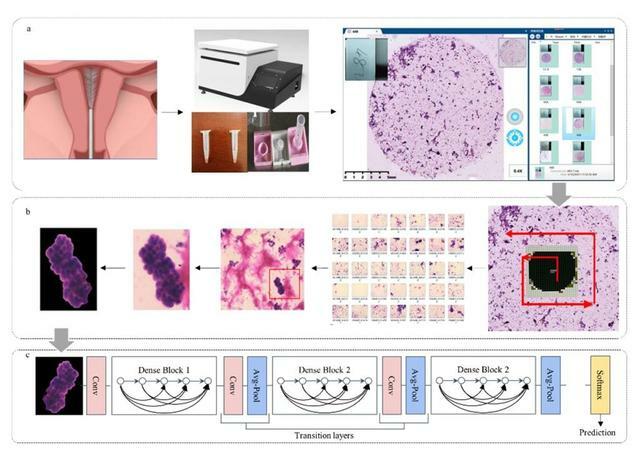
2022年8月26日,該研究成果以《基於深度卷積網絡的細胞群落病理診斷系統在子宮內膜癌篩查中的臨床應用》(Clinically Applicable Pathological Diagnosis System for Cell Clumps in Endometrial Cancer Screening via Deep Convolutional Neural Networks)為題,發表於腫瘤學1區雜誌《癌症》(Cancers)。論文共同第一作者為西安交大醫學部碩士生李清、西安交大自動化學院博士生王瑞潔,通訊作者為李奇靈教授、鍾德星副教授。2022年8月初,國家工業和信息化部、國家藥品監督管理局醫療器械註冊司組織的「人工智慧醫療器械創新任務揭榜」入圍單位名單揭曉,「子宮內膜癌細胞學篩查人工智慧輔助診斷系統」成為陝西唯一入圍「智能輔助診斷產品」方向的項目,標誌著本項目在子宮內膜篩查和人工智慧輔助診斷方面的創新突破獲得了國家級認可。
- 在ESD相關潰瘍快速修復研究取得重要進展
隨著消化道腫瘤早診早治觀念的興起與內鏡技術的不斷開展,ESD等消化內鏡超級微創技術已成為早期消化道癌、癌前病變、巨大息肉和黏膜下隆起病變的首選治療方法。然而,ESD術「人工潰瘍」成為最常見的影響患者生活質量的併發症,可導致患者出現腹痛、腹脹、消化不良、嘔血、便血等症狀。目前,對於ESD術後「人造潰瘍」的治療方法尚未達成共識。亟需尋找毒性較小、作用時間長、生物利用度高、適合全消化道黏膜損傷的新型治療方法。
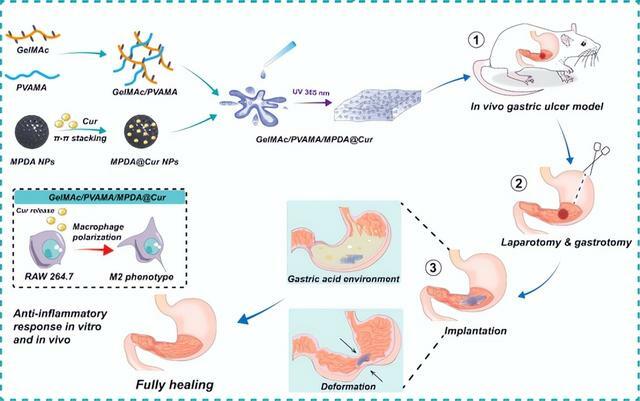
針對這一臨床難題,西安交大一附院消化內科和水祥主任團隊與重慶大學蔡開勇教授團隊合作,基於胃腸道特殊的生理環境和ESD術後創面的病理微環境特點,設計了一種包裹載薑黃素聚多巴胺納米顆粒的GelMAc/PVAMA水凝膠。成果以「Biocompatible, adhesive and stable GelMAc/PVAMA/MPDA@Cur hydrogels regulate immune response to improve endoscopic submucosaldissection-induced gastric ulcer healing in vivo」 為題,發表在生物材料權威期刊AppliedMaterials Today。西安交通大學第一附屬醫院消化內科張旭博士和美國杜克大學和野博士為論文共同第一作者,通訊作者為西安交通大學第一附屬醫院消化內科和水祥教授、任牡丹副教授和重慶大學蔡開勇教授。西安交通大學第一附屬醫院為第一和通訊單位。
- 在肝內膽管癌發病機制研究方面取得重要進展
為解析肝內膽管癌發展不同時期腫瘤組織內部的動態異質性,西安交通大學電信學部自動化學院葉凱教授與華中科技大學李蕾教授團隊建立肝內膽管癌小鼠模型,採集時序單細胞轉錄組數據,整合多維組學數據,分析驗證了調控腫瘤異質性的關鍵調控網絡、早期起源細胞、關鍵驅動基因、內皮纖維細胞在腫瘤發生發展過程中的動態相互作用。本研究報導的多種關鍵細胞類型和驅動基因提升了領域對肝內膽管癌的發病機制及瘤內異質性的認識,為診斷和治療提供了新的靶點。
該研究成果以「基於單細胞轉錄組的肝內膽管癌起始發展細胞異質性研究」(Cellular heterogeneity and transcriptomic profiles during intrahepatic cholangiocarcinoma initiation and progression)為題,發表在《肝病學》。西安交通大學為論文第一作者單位,西安交通大學電信學部自動化學院王庭傑博士生與華中科技大學徐傳瑞教授為共同第一作者。葉凱教授為末位通訊作者,李蕾教授為共同通訊作者。

- 在肝星狀細胞研究領域取得新進展
肝內膽管癌是第二常見的肝臟原發惡性腫瘤,僅次於肝細胞癌。西安交通大學第一附屬醫院肝膽外科劉青光教授研究團隊和美國明尼蘇達大學荷美爾研究所Ningling Kang教授研究團隊、美國梅奧醫學中心胃腸研究室Vijay H. Shah教授研究團隊共同合作,創新性發現PD-L1通過調節TGFβ受體I(TβRI)和TβRII促進肝星狀細胞轉變為腫瘤相關成纖維細胞。另外這項研究還建立了肝星狀細胞特異性缺失PD-L1的轉基因小鼠,通過把膽管癌細胞移植到這些小鼠的肝臟,發現肝星狀細胞特異性缺失PD-L1後,膽管癌在小鼠肝內的生長明顯受限。
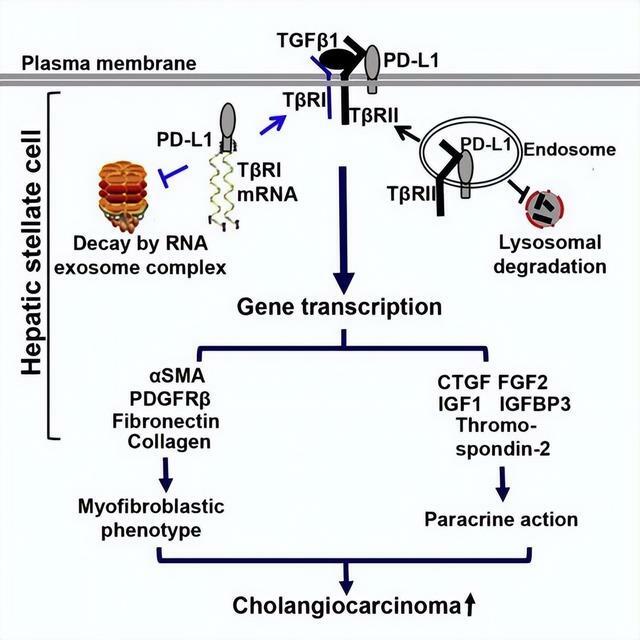
2022年2月8日,該研究成果在國際著名細胞生物學領域期刊《細胞通訊》(Cell Reports)發表,論文題目為《PD-L1通過對TGF-β受體I和II有選擇性的不同機制促進肝星狀細胞的肌成纖維細胞活化》(PD-L1 promotes myofibroblastic activation of hepatic stellate cells by distinct mechanisms selective for TGF-β receptor I versus II)。西安交通大學第一附屬醫院肝膽外科孫聯康博士為該文章的第一作者,劉青光教授和塗康生副研究員為參與作者,VijayH.Shah教授與NinglingKang教授為共同通訊作者。

- ……

防治癌症、改善癌症預後和提高患者生存質量是醫者的使命。接下來,西安交通大學及其附屬醫院將繼續創新探索、開闊視野,深入思考、凝心聚力,面向人民生命健康,不斷增強科技創新能力,提升科技競爭力,力爭在癌症相關領域的疾病診治、學科發展、人才培養等方面取得更顯著的成績。
關注「西安交通大學招生辦」,獲取關於國家首批985、211,雙一流建設高校——西安交通大學的最新精彩資訊!
素材來源:西安交通大學新聞網、福建衛生報、腫瘤醫學